日前,苏州大学神经科学研究所徐广银教授团队在《神经元》(Neuron)杂志上发表了题为“Distinct circuits andmolecular targets of the paraventricular hypothalamus decode visceral andsomatic pain”的研究论文。
该论文提出,下丘脑室旁核(paraventricular hypothalamus,PVH)作为“疼痛分拣中心”是大脑特异性识别传导内脏疼痛和躯体疼痛的关键中枢。研究发现,PVH以不同的神经元集群分别响应内脏疼痛和躯体疼痛,内脏疼痛和躯体疼痛所激活PVH神经元的转录组特征和下游投射模式存在显著差异,并通过PVHP2X3R+-LSV和PVHVIPR2+-ZIC神经环路差异性传导内脏疼痛和躯体疼痛。
疼痛是一种不愉快的感觉,被称为“第五大生命体征”,是机体自我防御的一种反应。近年来,人们对大脑高级中枢调节疼痛的神经环路和分子机制的认识取得了重大突破。然而,大脑特异性处理来自身体不同部位的痛觉信息并产生不同感觉和行为的具体机制仍未阐明。从位置上划分,疼痛有两个主要来源:内脏和躯体。内脏疼痛和躯体疼痛有密切的联系,并受到多个相同脑区的调控,但两者本质上是两种不同的痛觉形式。由于内脏和躯体的痛觉信息在大脑中被特异性识别编码的机制不明,目前临床上多数的镇痛药物和治疗手段无疼痛类型靶向性,对机体有较大的副作用。因此,探讨特异性识别传导内脏疼痛和躯体疼痛神经分子机制迫在眉睫。
针对如何在同一时空可视化内脏疼痛和躯体疼痛所激活的神经元,研究人员采用了Tet-off结合c-Fos染色的方法,并发现内脏疼痛和躯体疼痛激活PVH两群独立的神经元。通过功能依赖的激光显微切割捕获后RNA测序技术,发现被内脏疼痛和躯体疼痛所激活PVH神经元的转录组特征显著不同,P2X3R特异性高表达在内脏疼痛激活的神经元,而VIPR2特异性高表达在躯体疼痛激活的神经元。
基于功能依赖的病毒示踪方法,研究人员发现内脏疼痛和躯体疼痛所激活的PVH神经元具有不同的下游投射模式。内脏疼痛激活的PVH神经元对LSV(ventral part of lateral septal nucleus)存在大量投射,但几乎不投射至ZIC(caudal part of zona incerta)。相反的是,躯体疼痛激活的PVH神经元对ZIC存在大量投射,但几乎不投射至LSV。进一步的在体钙信号记录实验发现PVHP2X3R+-LSV通路特异性响应内脏疼痛刺激,而PVHVIPR2+-ZIC通路特异性响应躯体疼痛刺激,提示PVH-LSV和PVH-ZIC分别是特异性传导内脏疼痛和躯体疼痛的神经环路。
研究人员进一步通过化学遗传学方法证明了PVH-LSV和PVH-ZIC差异性调控内脏疼痛和躯体疼痛行为。最后,为探讨P2X3R和VIPR2是否分别基于PVH-LSV和PVH-ZIC神经环路发挥作用,研究人员通过shRNA敲降实验进行验证。
该研究不仅拓展了对大脑如何特异性识别不同位置来源疼痛的认识,还进一步揭示了差异性传导调控内脏疼痛和躯体疼痛的神经和分子机制,为临床上研发靶向治疗内脏疼痛和躯体疼痛的药物和干预手段提供了理论支撑。
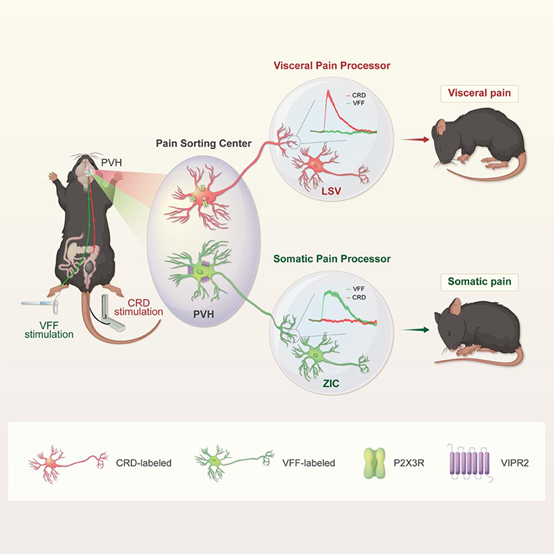
下丘脑室旁核差异性介导内脏疼痛和躯体疼痛的神经分子机制示意图
苏州大学神经科学研究所李永昌博士、张夫超博士为论文共同第一作者,徐广银教授为论文最后通讯作者。该研究得到了国家自然科学基金委(81920108016、32230041)、国家资助博士后研究人员计划等项目的资助。徐广银课题组近年来在内脏疼痛相关神经环路机制上取得了一系列进展,相关工作进一步拓展了对内脏疼痛的中枢神经与分子机制的理解,为相关疾病的精准诊疗提供了理论支撑。
论文链接:网页链接
苏州大学新媒体中心
素材来源:科学技术研究院、苏州医学院
整理编辑:赵晨欣